I.2. Disamina scientifica della tematica
I.2.1. Definizione

Per Contraccezione d’emergenza (CE) si intende l’assunzione di farmaci o l’inserimento di dispositivi intrauterini dopo il fallimento o il mancato utilizzo di un metodo contraccettivo durante un rapporto sessuale avvenuto nel periodo fertile del ciclo mestruale o dopo violenza sessuale.
1.2.2. Il ciclo ovarico
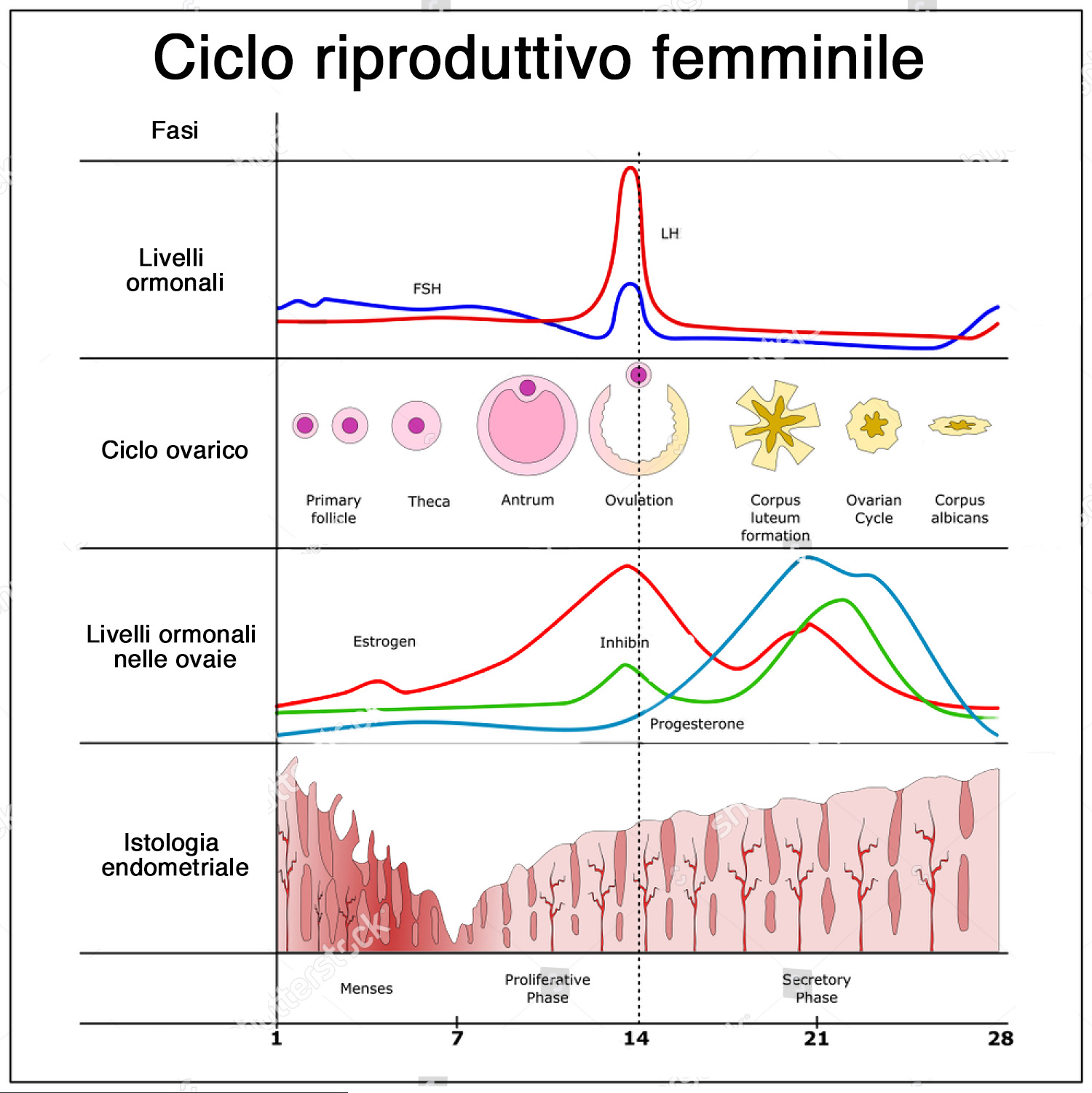
Il ciclo ovarico è caratterizzato da una sequenza di fenomeni, il centrale dei quali è l’ovulazione, regolati dalla sinergia di diversi ormoni. I principali ormoni prodotti dall’ovaio sono estrogeni e progesterone, la cui produzione è stimolata da altri ormoni di origine ipofisaria, in particolare l’ormone follicolo stimolante (FSH) e l’ormone luteinizzante (LH). Tutti sono in continuo dialogo biochimico con un feed back che armonizza gli eventi del ciclo ovarico. La loro quantità non è costante ma variabile a seconda del periodo. Nella prima fase del ciclo, la fase follicolare, aumentano FSH e LH. Il primo promuove la differenziazione del follicolo primario in follicolo secondario e stimola la conversione del testosterone in estrogeno, che ha il compito di supportare la crescita del follicolo. L’aumento dell’estrogeno determina un aumento progressivo fino ad un picco del LH che a sua volta mette in azione le sostanze che provocano la rottura del follicolo entro 13-16 ore.
La fertilità femminile è dunque ciclica ed è limitata al giorno dell’ovulazione, ai 4-5 giorni precedenti e al giorno successivo. La probabilità di concepimento è massima nel giorno che precede l’ovulazione e nello stesso giorno si ha anche la maggiore frequenza di rapporti sessuali.
Questi brevi cenni di fisiologia permettono di comprendere meglio il meccanismo d’azione dei contraccettivi d’emergenza.
I.2.3. Tipi di contraccezione d’emergenza
I dispositivi per la CE attualmente più utilizzati sono ormonali, rappresentati principalmente dal levonorgestrel, progestinico di sintesi, e dall’ulipristal acetato, antiprogestinico. L’utilizzo di dosi superiori a quelle giornaliere di un estroprogestinico, la classica “pillola”, suddiviso in due assunzioni distanziate da 12 ore e conosciuto come “metodo Yuzpe” è diminuito da quando sono state introdotte e soprattutto liberalizzate le pillole “del giorno dopo” e “dei cinque giorni dopo”.
Metodo contraccettivo d’emergenza non ormonale è lo IUD (Intra Uterine Device), la cosiddetta “spirale”, inserito entro 120 ore. Di questo è chiaro l’effetto antinidatorio.
I.2.4. Meccanismo d’azione
Del meccanismo d’azione della CE ormonale si è discusso negli ultimi anni e si discute tuttora.
La posizione ufficiale della HRA Pharma-azienda produttrice dell’ulipristal acetato utilizzato per la CE− e di società scientifiche autorevoli come la Food and Drugs Administration (FDA) statunitense, l’Agenzia Europea dei Medicinali (EMA), l’International Consortium for Emergency Contraception e l’International Federation of Gynecology & Obstetrics (FIGO), è attestata sull’affermazione che la CE inibisce o ritarda l’ovulazione, non essendoci dati che dimostrino effetti postconcezionali o abortivi3.
Anche il foglietto illustrativo di Ellaone al paragrafo «Come funziona ellaOne» recita:
Da più parti, tuttavia, è stato sollevato il dubbio che intervengano altri meccanismi d’azione, non ancora completamente noti ma atti a fornire una spiegazione meno semplicistica dell’efficacia della CE nel prevenire una gravidanza. Lo stesso Ministero della Salute, sentito il parere del Consiglio Superiore di Sanità, autorizzando in un documento del 2015 l’utilizzo dell’ulipristal acetato, afferma che «ritiene secondo i meccanismi d’azione del farmaco e la letteratura ancora controversa di non poter escludere un’azione antinidatoria». Contemporaneamente concorda una risk mitigation strategy per quanto riguarda l’utilizzo come contraccezione regolare, l’utilizzo più di cinque giorni dopo un rapporto sessuale non protetto, l’assunzione durante la gravidanza, l’allattamento al seno nella settimana successiva all’assunzione di EllaOne, l’utilizzo in donne affette da asma severa in trattamento con glucocorticoidi orali, l’utilizzo in donne con insufficienza epatica grave, l’utilizzo concomitante di levonorgestrel come contraccettivo di emergenza per lo stesso rapporto sessuale non protetto, l’uso concomitante di contraccezione ormonale, l’uso con induttori del CYP3A4. Ritiene infatti che debbano essere prese tutte le precauzioni affinché risulti improbabile un’assunzione ripetuta nel breve termine.
I.2.4.1. Levonorgestrel
Il levonorgestrel (LNG) è un progestinico di sintesi, derivato da 19-nortestosterone, che deve essere assunto usualmente in un’unica dose di 1.5 mg., da raddoppiare se sono stati assunti farmaci induttori enzimatici, entro 72 ore dal rapporto a rischio, anche più volte nello stesso ciclo. L’efficacia è massima nelle prime 12 ore e decresce nelle successive (95% nelle prime 24 ore, 85% fra le 24 e le 48 ore, 58% fra le 48 e le 72 ore) anche se sembra persistere fino a 96 ore.
È stato appurato che il meccanismo d’azione varia a seconda del periodo del ciclo in cui il LNG viene assunto e che solo prima del picco del LH può interrompere il processo ovulatorio4. Sarebbe quindi importante poter individuare con precisione il periodo del ciclo in cui si assume il LNG, ma nella vita quotidiana risulta difficile: non tutte le donne ricordano semplicemente la data dell’ultima mestruazione o sanno riconoscere i marcatori biologici dell’ovulazione per di più falsati dalla presenza dello sperma. Nella pratica clinica inoltre sarebbe impraticabile un routinario controllo seriato dei livelli ormonali o del diametro follicolare che chiarisca con sufficiente precisione la fase del ciclo. Occorre anche considerare che la liberalizzazione dell’acquisto dei contraccettivi di emergenza ha reso più facile la loro gestione da parte delle donne, molte delle quali hanno l’errata convinzione che abbiano un’efficacia del 100%.
Due studi hanno esaminato con monitoraggio ormonale ed ecografico complessivamente 492 donne che avevano utilizzato il LNG5. In particolare, lo studio di Noé e coll. del 2011 ha preso in esame 393 cicli datando l’ovulazione con monitoraggio ormonale ed ecografico. Il 99% delle donne aveva assunto 1.5 mg di LNG entro 72 ore dal rapporto sessuale non protetto. Nelle 148 donne che avevano avuto rapporti nel periodo fertile il numero di gravidanze previsto era di 24.7 ma se ne sono verificate 8. Nelle 103 donne che avevano assunto il LNG prima dell’ovulazione (dal giorno -5 al giorno -1) si è osservata una differenza significativa fra il numero di gravidanze attese, 16, e quello delle gravidanze iniziate, nessuna. Nelle 45 donne che avevano utilizzato il LNG nel giorno dell’ovulazione o dopo il numero di gravidanze previsto, 8.7, è risultato sovrapponibile a quello delle gravidanze insorte, 8. Questa incongruenza ha portato gli Autori a ipotizzare che il LNG agisca non soltanto ritardando l’ovulazione ma anche alterando altri fattori di fertilità come la qualità dello sperma, il transito tubarico o la recettività endometriale.
È stato anche ipotizzato che il LNG alteri il normale processo ovulatorio provocando una disfunzione ovulatoria, definita da Croxatto «una rottura del follicolo non preceduta da un picco di LH o preceduto da un picco di LH basso (<21 IU/l) o non seguita da un aumento del progesterone superiore a 12 nmol/l».
Un altro studio ha osservato negli spermatozoi esposti al LNG un’alterazione della motilità, aggravata anche dalla maggiore densità del muco cervicale, della capacitazione e della interazione con la zona pellucida dell’ovocita6.
Dati più recenti della letteratura attribuiscono al LNG anche un’interferenza nella funzionalità tubarica7. La fecondazione avviene normalmente nella zona ampollare della tuba circa 24 ore dopo l’ovulazione e ad essa segue il trasporto dello zigote attraverso la tuba per l’annidamento nell’utero. In questa fase sono fondamentali una corretta motilità della tuba dovuta alle contrazioni muscolari della parete ed un movimento delle ciglia armonico e sincrono. Un transito troppo lento o troppo rapido può causare una desincronizzazione degli eventi di questa prima delicatissima fase con conseguente fallimento dell’impianto dell’embrione. Alcuni studi hanno osservato una riduzione di frequenza del battito ciliare anche del 40-50% e della contrattilità muscolare delle tube che rallenterebbe il transito verso la cavità uterina del prodotto del concepimento con esito in aborto o gravidanza tubarica.
Un aumento delle gravidanze ectopiche è stato effettivamente riscontrato in donne che avevano utilizzato il LNG. In uno studio caso-controllo condotto in Kenia sono state comparate 79 donne con storia di gravidanza ectopica e 237 controlli. Nel primo gruppo è stata riportata una percentuale di assunzione di LNG (32.9%), significativamente superiore rispetto al secondo (7.2%) con un aumento di 9 volte di gravidanza tubarica nelle donne trattate con LNG rispetto a quelle che utilizzavano altri contraccettivi8.
Un case report pubblicato a febbraio 2019 riferisce due salpingectomie consecutive per gravidanze ectopiche in una donna che aveva assunto LNG ma presentava anche fattori di rischio quali un’infezione da Chlamydia ed endometriosi9.
Non sono stati invece dimostrati effetti sull’endometrio tali da impedire l’impianto dell’embrione o differenze di outcome della gravidanza fra donne che avevano o non avevano assunto LNG.
I.2.4.2. Ulipristal acetato
L’Ulipristal acetato (UPA) è attualmente considerato il contraccettivo di emergenza di prima scelta per l’efficacia più elevata rispetto al LNG. È in vendita sotto forma di una compressa, commercializzata come Ellaone, contenente 30 mg di principio attivo micronizzato da assumere entro 120 ore dal rapporto a rischio. Viene assorbito rapidamente e raggiunge il picco plasmatico dopo circa 1 ora. È metabolizzato a livello epatico ed ha una emivita di 32 ore. A fronte dell’ampia disponibilità vi sono delle limitazioni all’uso dell’UPA. È controindicato nelle donne con asma grave, ipersensibilità verso il principio attivo o gli eccipienti e soprattutto patologie epatiche.
Nel 2017 l’European Medicines Agency (EMA) ha avviato una revisione del farmaco contenente 5 mg di UPA da assumere per tre mesi continuativi per la cura dei fibromi uterini a seguito della segnalazione di quattro casi di grave danno al fegato, con esito in trapianto d’organo in tre. Il Comitato di valutazione dei rischi per la farmacovigilanza dell’EMA (PRAC) dopo una prima valutazione ha ritenuto che il farmaco potesse esserne la causa. Al termine della revisione il suo utilizzo è stato nuovamente autorizzato a condizione che venga controllata la funzionalità epatica prima, durante e dopo il ciclo di trattamento. Lo stesso documento dell’EMA afferma però che per Ellaone non sono stati segnalati casi di danno epatico.
Inoltre, possono interferire con l’UPA diminuendone l’efficacia farmaci induttori di enzimi epatici se assunti contemporaneamente o nel mese precedente. Alcuni di questi hanno un utilizzo più limitato come gli antiretrovirali e gli antiepilettici, altri sono di uso più comune come l’iperico, gli antiacidi e gli inibitori della pompa protonica per il trattamento dei disturbi gastrici. Inoltre, a sua volta l’UPA può ridurre l’effetto dei contraccettivi ormonali10.
Pur non essendo stato dimostrato un effetto teratogeno è consigliabile escludere la gravidanza prima dell’assunzione. Un’informativa dell’AIFA (Agenzia Italiana del Farmaco) del 16 marzo 2018 invita operatori sanitari e donne a segnalare gravidanze insorte con l’UPA:
La raccolta dei dati relativi al decorso della gravidanza e agli esiti perinatali permetterà di avere più informazioni sugli effetti dell’UPA sull’embrione e sul feto.
Le donne che allattano devono sospendere l’allattamento per almeno 36 ore.
Perché inizi la gravidanza occorre che si verifichi il rilascio dell’ovulo seguito dalla fecondazione e dall’annidamento dell’ovulo fecondato nell’utero. Il progesterone svolge un ruolo determinante nello scandire i tempi dell’ovulazione e preparare l’ambiente uterino all’impianto.
Il principio attivo di ellaOne, ulipristal acetato, agisce da modulatore del recettore del progesterone. Tanto l’UPA quanto il mifepristone, impiegato nell’interruzione volontaria farmacologica della gravidanza, hanno una struttura simile a quella del progesterone. Grazie a questa analogia l’UPA può legarsi ai recettori ai quali normalmente si lega il progesterone, impedendo così all’ormone di esercitare le sue funzioni. In questo modo agisce principalmente come antagonista del progesterone.

All’UPA viene riconosciuta la capacità di posporre l’ovulazione ma è stato dimostrato che questo fenomeno interviene solo se viene assunto prima del picco dell’LH, momento dell’ovulazione, e non nella fase luteale del ciclo, ad ovulazione già avvenuta. In uno studio di Brake e coll11 si afferma che se l’UPA viene somministrato quando il diametro follicolare è pari o superiore a 18 mm la rottura del follicolo viene evitata nel 59% dei casi, mentre il blocco o il ritardo dell’ovulazione si ha nel 100% dei casi quando il livello del LH è molto basso, nel 79% dei casi quando l’aumento del LH sta appena iniziando e in nessun caso durante il picco del LH. Le stesse informazioni vengono fornite in un documento congiunto della Società Italiana della Contraccezione (SIC) e della Società Medica Italiana per la contraccezione (SMIC)12. Per questo motivo fin dai primi periodi del suo utilizzo sono stati formulati dei dubbi sull’unicità di questo meccanismo d’azione13.
Studi successivi hanno messo in evidenza come l’UPA possa avere altri siti d’azione dell’UPA come le tube, lo sperma, l’endometrio. Una corretta funzionalità tubarica, come già ricordato, è indispensabile per la fecondazione ed il transito dello zigote. In alcuni studi è stata osservata un’inibizione della contrattilità della parete e del battito ciliare in seguito ad assunzione di UPA a dosi farmacologiche14.
Il progesterone influenza in modo rilevante la qualità del liquido seminale. Durante il loro percorso nelle vie genitali femminili gli spermatozoi sono esposti a livelli crescenti del progesterone prodotto dal corpo luteo e dalle cellule del cumulo ooforo. La presenza di progesterone nel fluido follicolare è indispensabile per la reazione acrosomiale, che permette allo spermatozoo di fecondare la cellula uovo. Poiché l’UPA è un antiprogestinico è stato dunque ipotizzato che possa inibire la capacità fecondante dello spermatozoo15.
Dopo l’ovulazione ciò che resta del follicolo diventa corpo luteo, il quale stimola la produzione del progesterone necessario a creare nell’endometrio le condizioni favorevoli all’impianto. Mediante biopsie eseguite a sei giorni dall’ovulazione è stato osservato un ritardo della maturazione dell’endometrio dopo assunzione di 50-100 mg di UPA ma non di 10 mg o di placebo16. Questo riscontro ha fatto concludere in un primo momento che la dose di UPA utilizzata per la CE non avesse un effetto significativo sulla recettività dell’endometrio. Tuttavia, si deve considerare che la somministrazione di 50 mg di UPA non micronizzato induce una significativa riduzione dello spessore dell’endometrio e che dal punto di vista farmacocinetico 30 mg di UPA micronizzato, contenuti in EllaOne, equivalgono a 50 mg di UPA non micronizzato. Ulteriore conferma dell’influenza dell’UPA sull’endometrio è arrivata dal riscontro di anomalie delle strutture ghiandolari e vascolari in seguito ad assunzione di 5 mg di UPA al giorno per tre mesi continuativi per il trattamento dei fibromi uterini17.
Analoghi risultati vengono riferiti da uno studio condotto con 12 utilizzatrici di un anello vaginale contraccettivo che rilasciava 1.5 o 2.5 mg di UPA al giorno. In ciascuna sono state eseguite 4 biopsie endometriali: una prima dell’inserimento dell’anello durante la fase luteale determinata con il dosaggio del LH, due ogni 3 mesi di utilizzo ed una un mese dopo la sospensione del metodo. Nella prima e nell’ultima biopsia si poteva osservare un endometrio normale, nelle due eseguite durante l’utilizzo dell’UPA si trovavano ghiandole endometriali con dilatazioni cistiche, disordini strutturali e secretori, stroma più compatto e non decidualizzato e vasi con ispessimento della parete18.
Questi studi starebbero quindi ad indicare che l’UPA non funziona solo ritardando l’ovulazione ma anche inducendo delle modificazioni dell’ambiente uterino che diventa non idoneo all’impianto dell’embrione. In questa direzione vanno anche studi più recenti. Uno del 2018 rileva come l’UPA, quando somministrato nel periodo periovulatorio può alterare il meccanismo che porta alla decidualizzazione dell’endometrio in risposta al progesterone nei giorni di massima recettività per l’embrione19.
In un altro studio pubblicato a maggio 2019 vengono confrontate le caratteristiche dell’endometriodi femmine di topo trattate con una dose di 40 mg/kg di UPA e quelle di animali non trattate. Nel primo gruppo ci sono state meno gravidanze rispetto ai controlli e a livello endometriale sono state osservate alterazioni istologiche e funzionali con una asincronia di sviluppo fra componente ghiandolare e stromale e incapacità di rispondere a tentativi di indurre artificialmente la decidualizzazione20.
La ricerca e la pratica clinica mettono tuttora in evidenza come la contraccezione d’emergenza sia un argomento di crescente complessità per le sue implicazioni biologiche, sociali ed etiche. Molti dei dubbi insorti inizialmente sul suo meccanismo d’azione sono stati sciolti dalle ricerche degli ultimi anni ma su questo argomento molte domande devono ancora essere poste e molte risposte devono ancora essere date.
Note
3 1) INTERNATIONAL FEDERATION OF GYNECOLOGY & OBSTETRICS, INTERNATIONALE CONSORTIUM FOR EMERGENCY CONTRACEPTION: EMERGENCY CONTRACEPTION STATEMENT: How do Levonorgestrel-Only Emergency Contraceptive Pills Prevent Pregnancy? Some Considerations, in «Gynecol Endocrinol» 2011
2) INTERNATIONAL FEDERATION OF GYNECOLOGY & OBSTETRICS, International Consortium for Emergency Contraceptive Pills. Medical and Service Delivery Guidelines, 2012
4 K. CLEVELAND, EG. RAYMOND, E. WESLEY, J. TRUSSEL, Emergency Contraception Review: Evidence-based Recommendations for Clinicians, in «Clin Obstet Gynecol.» 2014 Dec; 57 (4): 741-50
5 G. NOÉ, HB CROXATTO, AM SALVATIERRA et al., Contraceptive Efficacy of Emergency Contraception with Levonorgestrel Given Before or After Ovulation, in «Contraception» 2011; 84:486-492; N. NOVIKOVA, E. WEISBERG, FZ STANCZYK et al., Effectiveness of Levonorgestrel Emergency Contraception Given Before of After Ovulation – A Pilot Study, in «Contraception» 2007; 75:112-118 ⌈PubMed⌉ ⌈Google Scholar⌉
6 M. CHIRINOS, M. DURAND, ME GONZÁLEZ-GONZÁLEZ, G. HERNÁNDEZ-SILVA, I. MALDONADO-ROSAS, P. LÓPEZ, F. LARREA, Uterine Flushings from Women Treated with Levonorgestrel Affect Sperm Functionality in Vitro, in «Reproduction» 2017 Nov; 154 (5):607-614; doi: 10.1530/REP-17-0313; Epub 2017 Sep 8
7 C. LI, H. ZHANG, Y. LIANG, W. XIA, Q. ZHU, D. ZHANG, Z. HUANG,GL LIANG, RH XUE, H. QI, HE XQ, JJ YUAN, YJ TAN, HF HUANG, J. ZHANG, Effects of Levonorgestrel and Progesterone on Oviductal Physiology in Mammals, in «Reprod Biol Endo-crinol.» 2018 Jun 20; 16 (1):59
8 S. SHURIE, E. WERE, O. ORANG’O, A. KETER, Levonorgestrel Only Emergency Contraceptive Use and Risk of Ectopic Pregnancy in Eldoret Kenya: A Case-Control Study , Published online 2018 Nov 29; doi: 10.11604/pamj.2018.31.214.17484
9 Y. KITANI, T. ISHIGURO, A. KOBAYASHI, R. TAMURA, H. UEDA, S. ADACHI, N. NISHIKAWA, M. SEKINE, T. ENOMOTO, Ectopic Pregnancy Following Oral Levonorgestrel Emergency Contraception Use, in «Obstet Gynaecol Res.» 2019 Feb; 45 (2):473-476; doi: 10.1111/jog.13815; Epub 2018 Sep 23
10 AB EDELMAN, JP JENSEN, S, MCCRIMMON, M. MESSERIE-FORBES, A. O’DONNEL, JD HENNEBOLD, in Combined Oral Contraceptive Interference with the Ability of Ulipristal Acetate to Delay Ovulation: A Prospective Cohort Study, in «Contraception» 2018 Dec; 98 (6): 463-466
11 V. BRAKE et al., Immediate Pre-ovulatory Administration of 30 mg of Ulipristal Acetate Taken Significantly Delays Follicular Rupture, in «Hum Reprod.» 2010; 25: 2256-63
12 SIC-SMIC, Ulipristal Acetato. Un nuovo farmaco per la contraccezione d’emergenza: aspetti clinici, medico-legali e percorsi di utilizzo, Febbraio 2012
13 E. ROSATO, M. FARRIS and C. BASTIANELLI, Mechanism of Action of Ulipristal Acetate for Emergency Contraception: A Systematic Review, in «Front Pharmacol.» 2015; 6: 315
14 HW LI, SB LIAO, WS YEUNG, EH NG, WS O, PC HO, Ulipristal Acetate Resembles Mifepristone in Modulating Human Fallopian Tube Function, in «Hum. Reprod.» 2014; 29: 2156–2162; J. YUAN, W. ZHAO, M. YAN, Q. ZHU, G. QIN, J. QIU et al., Ulipristal Acetate Antagonizes the Inhibitory Effect of Progesterone on Ciliary Beat Frequency and Upregulates Steroidex Pression Levels in Human Fallopian Tubes, in «Reprod. Sci.» 2015; 22: 1516–1523
15 JKY KO, VW HUANG, RHW LI, WSB YEUNG, PC HO, PCN CHIU, An in Vitro Study of the Effect of Mifepristone and Ulipristal Acetate on Human Sperm Functions, 2014 Nov; 2(6): 868–874; doi: 10.1111/j.2047-2927.2014.00261.x
16 P. STRATTON, ED LEVENS, B. HARTOG, J. PIQUION, Q. WEI, M. MERINO et al., Endometrial Effects of a Single Early Luteal Dose of the Selective Progesterone Receptor Modulator CDB-2914, in «Fertil.Steril.» 2010 Apr; 93: 2035–2041; doi: 10.1016/j.fertnstert.2008.12.057
17 AR Williams, C. BERGERON, DH BARLOW, A. FERENCZY, Endometrial Morphology After Treatment of Uterine Fibroids with the Selective Progesterone Receptor Modulator, Ulipristal Acetate, in «Int. J. Gynecol. Pathol.» 2012; 31: 556–569
18 S. LIRA-ALBARRÁN, M. DURAND, D. BARRERA, C. VEGA, RG BECERRA, L. DÍAZ, J. GARCÍA-QUIROZ, C. RANGEL, F, LARREA, A single Pre-Ovulatory Administration of Ulipristal Acetate Affects the Decidualization Process of the Human Endometrium During the Receptive Period of the Menstrual Cycle, in «Mol Cell Endocrinol.» 2018 Nov 15; 476: 70-78
19 AR WILLIAMS, C, BERGERON, DH BARLOW, A. FERENCZY, Endometrial Morphology After Treatment of Uterine Fibroids with the Selective Progesterone Receptor Modulator, Ulipristal Acetate, in «Int. J. Gynecol. Pathol.» 2012; 31: 556–569
20 MD GÓMEZ-ELÍAS, M. MAY, MJ MUNUCE, L. BAHAMONDES, PS CUASNICÚ, DJ COHEN, A Single Post-Ovulatory Dose of Ulipristal Acetate Impairs Post-Fertilization Events in Mice, in «Mol Hum Reprod» 2019 May 1; 25 (5):257-264
Bibliografia
BRAKE V. et al., Immediate Pre-Ovulatory Administration of 30 mg of Ulipristal Acetate Taken Significantly Delays Follicular Rupture, «HumReprod» 2010, 25: 2256-63
CHIRINOS M., DURAND M., GONZÁLEZ-GONZÁLEZ ME, HERNÁNDEZ-SILVA G., MALDONADO-ROSAS I., LÓPEZ P., LARREA F., Uterine Flushings from Women Treated with Levonorgestrel Affect Sperm Functionality in Vitro, in «Reproduction» 2017 Nov; 154 (5):607-614; doi: 10.1530/REP-17-0313; Epub 2017 Sep 8
CLEVELAND K., RAYMOND EG, WESLEY E., TRUSSEL J., Emergency Contraception Review: Evidence-based Recommendations for Clinicians, in «Clin Obstet Gynecol.» 2014 Dec; 57 (4): 741-50
EDELMAN AB, JENSEN JP, MCCRIMMON S., MESSERIE-FORBES M., O’DONNEL A., HENNEBOLD JD, Combined Oral Contraceptive Interference with the Ability of Ulipristal Acetate to Delay Ovulation: A Prospective Cohort Study, in «Contraception» 2018 Dec; 98 (6): 463-466
MD GÓMEZ-ELÍAS, M. MAY, MJ MUNUCE, L. BAHAMONDES, PS CUASNICÚ, DJ COHEN, A Single Post-Ovulatory Dose of Ulipristal Acetate Impairs Post-Fertilization Events in Mice, in «Mol Hum Reprod» 2019 May 1; 25 (5):257-264
INTERNATIONAL FEDERATION OF GYNECOLOGY & OBSTETRICS, International Consortium for Emergency Contraception: EMERGENCY CONTRACEPTION STATEMENT: How do Levonorgestrel-Only Emergency Contraceptive Pills (LNG ECPs) Prevent Pregnancy?, in «Gynecol Endocrinol» 2011 Jun; 27(6): 439-42
INTERNATIONAL FEDERATION OF GYNECOLOGY & OBSTETRICS, INTERNATIONAL CONSORTIUM FOR EMERGENCY CONTRACEPTION, Emergency Contraceptive Pills. Medical and Service Delivery Guidelines, New York London 2012
KITANI Y., ISHIGURO T., KOBAYASHI A., TAMURA R., UEDA H., ADACHI S., NISHIKAWA N., M. SEKINE, ENOMOTO T., Ectopic Pregnancy Following Oral Levonorgestrel Emergency Contraception Use, in «Obstet Gynaecol Res.» 2019 Feb; 45 (2):473-476; doi: 10.1111/jog.13815; Epub 2018 Sep 23
KO JKY, HUANG WV, LI RHW, YEUNG WSB, HO PC, CHIU PCN, An in Vitro Study of the Effect of Mifepristone and Ulipristal Acetate on Human Sperm Functions 2014 Nov; 2(6): 868–874; doi: 10.1111/j.2047-2927.2014.00261.x
LI C., ZHANG H., LIANG Y., XIA W., ZHU Q., ZHANG D., HUANG Z., LIANG GL, XUE RH, QI H., XQ HE, YUAN JJ, TAN JY, HUANG HF, ZHANG J., Effects of Levonorgestrel and Progesterone on Oviductal Physiology in Mammals, in «Reprod Biol Endo-crinol.» 2018 Jun 20; 16 (1):59
LI HW., LIAO SB., YEUNG WS, NG EH, O WS, HO PC, Ulipristal Acetate Resembles Mifepristone in Modulating Human Fallopian Tube Function, in «Hum. Reprod.» 2014; (29): 2156–2162
LIRA-ALBARRÁN S., DURAND M., BARRERA D., VEGA C., BECERRA RG, DÍAZ L., GARCÍA-QUIROZ J, RANGEL C., LARREA F., A single Pre-Ovulatory Administration of Ulipristal Acetate Affects the Decidualization Process of the Human Endometrium During the Receptive Period of the Menstrual Cycle, in «Mol Cell Endocrinol.» 2018 Nov 15; 476: 70-78
NOÉ G., CROXATTO HB, SALVATIERRA AM et al., Contraceptive Efficacy of Emergency Contraception with Levonorgestrel Given Before or After Ovulation, in «Contraception» 2011; 84: 486-492
NOVIKOVA N., WEISBERG E., STANCZYK FZ et al., Effectiveness of Levonorgestrel Emergency Contraception Given Before of After Ovulation – A Pilot Study, in «Contraception» 2007; 75:112-118 ⌈PubMed⌉ ⌈Google Scholar⌉
ROSATO E., FARRIS M. and BASTIANELLI C, Mechanism of Action of Ulipristal Acetate for Emergency Contraception: A Systematic Review, in «Front Pharmacol.» 2015; 6: 315
SHURIE S., WERE E., ORANG’O O., KETER A., Levonorgestrel Only Emergency Contraceptive Use and Risk of Ectopic Pregnancy in Eldoret Kenya: A Case-Control Study , Published online 2018 Nov 29; doi: 10.11604/pamj.2018.31.214.17484
SIC-SMIC, Ulipristal Acetato. Un nuovo farmaco per la contraccezione d’emergenza: aspetti clinici, medico-legali e percorsi di utilizzo, Febbraio 2012: 1-6
STRATTON P., LEVENS ED, HARTOG B., PIQUION J., WEI Q., MERINO M. et al., Endometrial Effects of a Single Early Luteal Dose of the Selective Progesterone Receptor Modulator CDB-2914, in «Fertil.Steril.» 2010 Apr; 93: 2035–2041; doi: 10.1016/j.fertnstert.2008.12.057
WILLIAMS AR, BERGERON C., BARLOW DH, FERENCZY A., Endometrial Morphology After Treatment of Uterine Fibroids with the Selective Progesterone Receptor Modulator, Ulipristal Acetate, in «Int. J. Gynecol. Pathol.» 2012; 31: 556–569
YUAN J., ZHAO W., YAN M., ZHU Q., QIN G., QIU J. et al., Ulipristal Acetate Antagonizes the Inhibitory Effect of Progesterone on Ciliary Beat Frequency and Upregulates Steroidex Pression Levels in Human Fallopian Tubes, in «Reprod. Sci.» 2015; 22: 1516–1523
© Bioetica News Torino, Giugno 2020 - Riproduzione Vietata